|
reklama
| Transplantace jater u dětí |
|
MUDr. Libor Janoušek Ph.D. |
| SANQUIS č.89/2011, str. 72 |
 |
zpět na výběr odborných článků |
První transplantaci jater u dítěte provedl Thomas E. Starzl v roce 1963 v Denveru. Příčinou selhání jater byla u tohoto pacienta biliární atrézie, tedy vrozená vada žlučových cest, které se nevyvinuly. V dalších letech se transplantace jater stala léčebnou metodou při selhání jater u dětských pacientů.
|
|
|
Díky rozvoji a ustálení chirurgických technik a objevení nových, účinnějších imunosupresivních léků transplantací přibývalo, přesto ale byla dlouho úmrtnost dětí na čekací listině vysoká. Zatímco u dospělých se podařilo do 90. let minulého století snížit úmrtnost na čekací listině řádově na procenta, dětská úmrtnost se pohybovala mezi 30–50 %. Tento nepříznivý stav byl způsoben relativním nedostatkem vhodných štěpů jater pro dětské příjemce – dárce jater musí vyhovat kromě krevní skupiny i velikostně. U dětských pacientů se tím neúměrně prodlužovalo čekání na transplantaci. Proto odborníci hledali nové techniky, směřující k úpravě dostupných dospělých jaterních štěpů pro potřeby dětských příjemců. Tak vznikla technika redukce jaterního štěpu. První transplantaci redukovaným štěpem provedl Bismuth ve Francii a metoda se rychle rozšířila po celém světě. Úmrtnost dětí na čekací listině se snížila až na hodnoty 2–3 %.
Operační postup redukce dospělého štěpu vychází ze znalosti anatomických struktur jater, které poprvé popsal Couinaud. Identifi koval osm segmentů jater a jejich krevní a žlučové zásobení. To umožnilo použít k transplantaci pouze část jater velikostně vhodnou pro dítě. Zbývající část jater se k transplantaci nepoužila. Úspěšnost redukce štěpů a zvyšující se počet těchto transplantací vedl k upřednostňování dětských příjemců před dospělými, ačkoli ti představují jen desetinu všech transplantovaných pacientů. Řešení situace přinesl vývoj dalších postupů, které maximálně využívaly všech jaterních štěpů. Vznikla technika splitování jater, spočívající v rozdělení štěpu na dvě funkční části, izolovaně transplantované dvěma příjemcům – obvykle dospělému a dítěti. První split provedl Pichlmayer v Německu a brzy jej následovala další evropská a světová centra.
Po rozvoji této metody transplantace a s trvajícím nedostatkem vhodných dárců došlo k poslednímu kroku, kterým byl vývoj chirurgických technik příbuzenského odběru jater. První úspěšnou příbuzenskou transplantaci jater provedl Strong v roce 1989. Tak jako u splitování se využije pouze část jater a dárcem je v naprosté většině případů jeden z rodičů. Výhodu znamená kratší čekací doba a možnost výkon naplánovat. Dárce je také velmi pečlivě vyšetřen. Nevýhodu představuje etická otázka, kdy se rozhodujeme, zda máme „poškodit a zatížit“ operačním výkonem zdravého člověka. Malým, ale nezanedbatelným rizikem jsou možné chirurgické komplikace u těchto žijících dárců. Úmrtnost během příbuzenského odběru jater (!) se udává mezi 0,02–1 % a vznik komplikace vyžadující další operaci mezi 1–5 %. V České republice máme rozvinutý program zemřelých dárců orgánů a kratší čekací doby na transplantaci, proto na našem pracovišti využíváme příbuzenského odběru jater minimálně.
První transplantaci jater provedl v tehdejším Československu brněnský tým II. chirurgické kliniky vedený Vladimírem Kořístkem v roce 1983. V pražském Institutu klinické a experimentální medicíny se játra transplantují od roku 1995, v roce 1998 zde byla provedena první transplantace dítěte redukovaným štěpem. Od roku 2007 probíhá program jaterních transplantací velmi malých příjemců (pod 10 kg), odesílaných do této doby k transplantaci do zahraničí. V České republice se v současnosti programem transplantací jater systematicky zabývá Centrum kardiovaskulární a transplantační chirurgie (dále CKTCH) v Brně a Institut klinické a experimentální medicíny (dále IKEM) v Praze.
|
|
|
Onemocnění vedoucí k transplantaci
Hlavním a nejčastějším onemocněním vedoucím u dětí k selhání jater a transplantaci je biliární atrézie – vrozené onemocnění, při kterém se žlučové cesty buď částečně, nebo úplně nevyvinuly. Postihuje přibližně jednoho pacienta z 8–10 tisíc. Toto onemocnění můžeme od roku 1959 léčit tzv. Kasaiovou operací, při které se našívá klička tenkého střeva do místa odstupu nejmenších žlučových větví z jater. Tato operaci je úspěšná asi u 40–60 % nemocných. Nicméně 75 % takto operovaných pacientů stejně dospěje v pozdějším věku k transplantaci. Výhodou operace je nicméně odložení zákroku do pozdějšího věku, kdy velikost cévních struktur dává větší šanci na technickou úspěšnost transplantace. Dalším onemocněním postihujícím žlučové cesty je Alagillův syndrom. Vyznačuje se postižením žlučových cest v játrech spolu s vrozenými anomáliemi srdce a plic.
Vrozené metabolické poruchy tvoří další velkou skupinu onemocnění postihujících játra u dětí. Nejčastější z nich je defi cit enzymu α1 antitrypsinu. Jiným vrozeným onemocněním je tyrosinémie, porucha metabolismu aminokyselin. Dědičnou Wilsonovu chorobu charakterizuje ukládání mědi do jater, očí, ledvin, mozku a jiných orgánů. Z méně častých metabolicky podmíněných onemocnění lze ještě vyjmenovat Crigler-Najjarův syndrom, poruchy ukládání glykogenu a metabolismu lipidů.
Akutní selhání jater u dětí způsobuje jednak rozvoj základní nemoci, nebo častěji otrava léky či houbami. Poslední skupinu onemocnění vedoucích k transplantaci představují jaterní nádory. Nejčastější z nich, hepatoblastom, je spíše lokálně agresivní a metastazuje pozdně, hepatocelulární karcinom naopak patří mezi rychle rostoucí a metastazující nádory. K transplantaci jsou indikováni pacienti, u kterých nedošlo k rozšíření nádoru do těla a u nichž nejde nádor chirurgicky odstranit ani ovlivnit chemoterapií. Transplantace těchto pacientů mívají vynikající krátkodobé výsledky, dlouhodobé bohužel snižuje možnost recidivy.
Mezi okolnosti zcela vylučující transplantaci u dětí patří HIV pozitivita, nekontrolovatelná infekce organismu, selhání nebo život ohrožující onemocnění mimojaterních orgánů a samozřejmě zhoubné onemocnění mimo vlastní játra. Relativních překážek pro provedení zákroku je mnoho, řadí se sem zejména vrozená onemocnění srdce, plic a postižení centrálního nervového systému. Tehdy je třeba pečlivě zvažovat možnost vratnosti postižení orgánů mimo jaterní tkáň a kvalitu života po transplantaci.
Pooperační péče a možné komplikace
Nejrizikovější a nejzranitelnější skupinou našich pacientů jsou děti kojeneckého věku. Vyplývá to z nezralosti jejich organismu, nepříznivého poměru povrchu těla a hmotnosti, úzkých dýchacích cest pokrytých křehkou sliznicí, sníženou koncentrační schopností ledvin, bráničním dýcháním a mnoha jinými faktory. V pooperačním průběhu se tímto zvyšuje nebezpečí dehydratace, iontové nerovnováhy, prochladnutí, snižují možnost dechové rehabilitace a vedou k odlišnému vstřebávání léků.
Po operačním výkonu jsou pacienti hospitalizováni na Resuscitačním oddělení KARIP IKEM, kde monitorujeme základní životní funkce. Pravidelně se sleduje stav vnitřního prostředí a laboratorně a sonografi cky sledujeme funkci jaterního štěpu. Podáváme imunosupresivní léčbu – léky potlačující odhojovací reakci organismu. Dále dítě dostává antibiotika. Pravidelně se odebírají mikrobiologické stěry, aby se mohla včas zachytit infekce. Důraz v pooperační péči je kladen na udržení tělesné teploty, zajištění krevní srážlivosti, hrazení tekutin a krevních derivátů k zabezpečení oběhové stability a produkce moči.
|
|
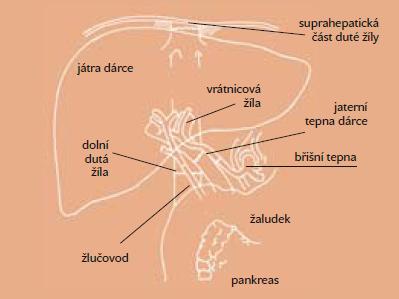 | | Schematické zobrazení transplantace jater |
|
|
Komplikace lze rozdělit na chirurgické a nechirurgické. Z chirurgických komplikací je nejčastější trombóza neboli uzávěr jaterní tepny. Vyskytuje se až ve 30 %. Napravit jej lze chirurgicky. Jinou častou komplikací je únik žluči nebo zúžení žlučovodu (do 25 %). Léčba spočívá v přešití žlučové anastomózy nebo zavedení speciální výztuhy – stentu. Vyskytnout se dále může stenóza či uzávěr portální žíly nebo jaterních žil (do 10 %). Řeší se operativně nebo perkutánní angioplastikou.
Z nechirurgických komplikací je třeba jmenovat odhojovací reakci organismu příjemce. S akutní rejekcí se setkáváme až u 30 % pacientů časně po transplantaci. Symptomy zahrnují teploty, bolest u štěpu, zvýšení hodnot jaterních enzymů a pokles syntetické funkce jater. Potvrdit diagnózu lze odebráním bioptického vzorku z jater. Léčba spočívá v podání kortikoidů nebo antilymfocytárních protilátek. Chronická rejekce se vyskytuje u 5–10 % transplantovaných dětí. Je nezvratná a postupný zánik žlučovodů a vazivovatění jaterní tkáně může ústit v retransplantaci.
Oslabený organismus dětí spolu s velkým operačním výkonem a pooperačním podáváním imunosuprese zvyšují výskyt infekcí po transplantaci. Proti některým patogenům se snažíme konkrétně zasáhnout podáváním antibiotik a očkováním. Podle typu infekce a míry rozšíření se spektrum obtíží pohybuje od trávicích problémů a zhoršení funkce jater, pneumonii, útlum kostní dřeně až po multiorgánové selhání a postižení centrálního nervového systému.
Zkušenosti z praxe
Od zahájení programu transplantací jater u dětí v IKEM v roce 1995 do roku 2010 bylo operováno 62 dětí ve věku 0–18 let. U těchto dětských příjemců bylo provedeno 68 transplantací, z toho 18 v zahraničí u nejmenší váhové kategorie, než jsme v roce 2007 převzali i tento nejobtížnější program. Od roku 2007 do roku 2010 bylo v IKEM transplantováno 11 dětí ve váhové kategorii do 15 kg. Z těchto 11 dětí jich přežívá s funkčním štěpem 10. Jeden pacient zemřel na nezvratné poškození mozku vzniklé zřejmě již před transplantací. Přežívání štěpů jater a příjemců je vyšší a výskyt chirurgických komplikací je v našem souboru dětských transplantovaných pacientů nižší ve srovnání se zahraniční literaturou. Plné znění článku viz www.sanquis.cz
|
|
|
Ilustrace vlevo: Dreamstime, schéma – archiv autora, graf – výroční zpráva TC IKEM 2010
|
|
|
 |
obsah čísla 89 |
 |
ročník 2011 |
 |
témata |
|
|



