| Granát odražený papírem |
|
František Houdek |
| SANQUIS č.84/2010, str. 56 |
| „Teď už vím, jak vypadá atom!“ S tímto prohlášením vtrhl jednoho těsně předvánočního dne roku 1910 Ernest Rutherford do pracovny svého německého postdoktoranda Hanse Geigera. No, tak docela to ještě nevěděl, nicméně stejně šlo o jeden z nejsilnějších, přestože nejstručnějších výroků v dějinách fyzikálního poznání. Ale vezměme to po řadě.
|
|
Někdy na jaře 1909 Rutherforda, v té době osmatřicetiletého profesora na univerzitě v Manchesteru (původem farmářského synka z Nového Zélandu, nyní už nositele Nobelovy ceny za chemii z roku 1908) zaujal jev, který zpočátku považoval za ryze otravný – rušil mu měření. S Geigerem totiž postavili dlouhou trubici, do které nechali vlétat částice alfa ze zdroje, těžkého radioaktivního prvku radia. V trubici mohli částice pozorovat a počítat. Vadilo jen to, že částice se často odchylovaly od původně přímočarých drah. Jenže místo aby se Rutherford snažil tento jev potlačit, začal jej studovat.
Přesněji řečeno, pověřil tím Hanse Geigera a Ernesta Marsdena, talentovaného krajana. Ten vzpomínal: „Rutherford se na mě obrátil se slovy: Co kdybyste zkusil zjistit, zda mohou být alfa částice odráženy pevnou kovovou látkou? Nečekám od toho sice nic moc zajímavého, ale pro jistotu se na to tu a tam mrkněte.“ Geiger s Marsdenem tedy ostřelovali fólie z různých kovů proudem tzv. helionů – ony částice alfa jsou rychle letící holá jádra izotopu helium 4. Podle tehdejších představ měly atomy vypadat jako kladně nabité homogenní kuličky, v nichž jako rozinky v pudinku „plovalo“ odpovídající množství záporných elektronů. V takovém případě by průletů částic alfa ubývalo úměrně s tloušťkou prolétané vrstvy. Jenže – třeba u zlaté fólie, tenounké pouhou tisícinu milimetru, sice drtivá většina helionů dle očekávání rovně prosvištěla, avšak asi jedna osmitisícina se navzdory vysoké pohybové energii velmi odchýlila ze směru letu či dokonce odrazila zpátky.
Rutheford později napsal: „Byl to určitě nejneuvěřitelnější výsledek, který jsem kdy v životě dostal. Bylo to skoro tak neuvěřitelné, jako kdyby někdo vystřelil patnáctipalcový granát proti listu hedvábného papíru a ten granát se vrátil a trefil jeho samotného!“
|
|
|
Planetární model
Uběhlo půldruhého roku. Poslední předvánoční víkend přesně před sto lety se Rutherford dovtípil: Atom není homogenní útvar, jak se myslelo dosud, nýbrž sestává z malého, velmi hmotného, neprůchodného jádra, kolem kterého relativně daleko obíhají nepatrné elektrony a svými drahami vymezují objem atomu. Mezi jádrem a elektrony – nicota. Z četnosti odrazů částic a tloušťky i druhu kovu fólie badatel dokonce vypočítal přibližný rozměr jádra. Rutherfordovu modelu se brzy začalo říkat planetární; koneckonců podobnost se sluneční soustavou (Slunce – jádro, planety – elektrony) se přímo nabízela.
Co Rutherford onen předvánoční pondělek ještě nevěděl: jaké povahy jsou jádro i síly, které částice ovlivňují? Jsou to síly gravitační jako ve vesmíru, nebo jde spíš o síly elektrické? Přesné okolnosti, za nichž to Rutherfordovi došlo, nejsou zřejmé, určitě v tom ale hrál roli již známý záporný náboj elektronů. Každopádně v květnu 1911, kdy Rutherford ideu planetárního modelu zveřejnil, bylo už všechno jasné: jádro atomu obsahuje velmi hmotné kladné částice (protony), kolem něho pak kolotají lehounké záporné elektrony. Jakkoli je dnes představa planetárního modelu atomu dávno překonána, i díky ní se zrodila atomistika moderního střihu, jeden ze základů dnešní velkolepé „kuchařky mikrosvěta“ – kvantové mechaniky.
Ernest Rutherford na sklonku světové války, už na staroslavné Cambridgi, ještě jako první na světě provedl umělou přeměnu jednoho chemického prvků v druhý. Další Nobelovu cenu prý odmítal se slovy: „Dejte ji raději některému z mých žáků!“
|
|
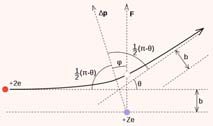 | | Schematicky vyznačený rozptyl alfa částic
v Rutherfordově modelu |
|
|
|
|
|
 |
obsah čísla 84 |
 |
ročník 2010 |
 |
témata |
|

| SANQUIS PLUS |

|
| GALERIE SANQUIS |

|
| PORADNA |

|
|



